认 证:工商信息已核实
访问量:530690

上海矽诺国际贸易有限公司 2020-05-25 点击848次
正极材料
锂离子电池正极材料作为其关键的组成部分,决定了电池的开路电势。为了提高锂离子电池的开路电压,锂离子电池中过渡金属的氧化态必须要高,以确保锂离子的电化学电势较高,从而尽量提高电池电压。同时正极材料内部结构中需要有充分的空间容纳锂离子,保证锂离子在嵌入/脱出的可逆过程中阻碍较少,尽量较少破坏内部结构中过渡金属与阴离子的化学键,使结构尽可能稳定。不仅如此,正极材料还应具备良好的电子和离子传导性,以保证较高的电流密度。目前锂离子电池正极材料有以下几种:
A.
层状化合物
以目前常用的 Li Co O2为代表的 Li MO2(M=V、Cr、Co 或 Ni)层状化合物正极材料。其层状化合物晶体结构中,Li+层和
M3+层占据了交替的[1 1 1]面,沿着 C 轴形成了-O-Li-O-M-O-Li-O-M-O 的规则排列[14,15]
。这样的结构在二维方向上有利于结构的稳定,并且通过与过渡金属直接相互作用提高了材料的电导率,减少了多次反复充放电带来的体积变化。
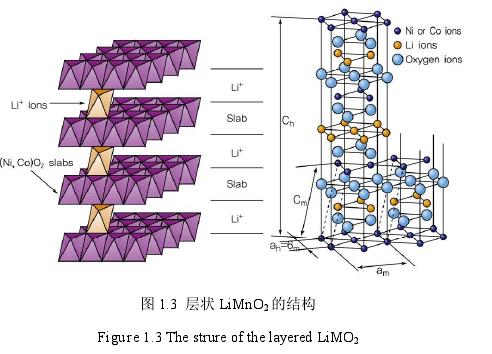
层状化合物 Li MO2正极材料的结构如图 1.3 所示。由过渡金属离子和氧形成的锂氧八面体和氧化层的相互交替排列形成了较强的离子键,但在 MO2层之间的库伦排斥力使得锂离子可以较为自由的嵌入与脱出,从而使得层状化合物Li MO2在二维平面方向的离子电导性得到大幅度提高[16]。
充电过程中,正极材料的锂离子脱出,在结构中产生八面体空位,邻近的锂离子从而可以依次扩散和脱出。放电时锂离子可以重新嵌入结构中的八面体空位。
由于 MO2层中的氧原子相互排斥,在充电过程中锂离子脱出会造成晶格的膨胀,从而使得 Li MO2在 C 轴方向收缩[17]。在充电过程中锂含量的变化,使得 Li MO2重新形成稳定的晶体结构,从而正极材料的特性也得以保持。
尖晶石化合物
在一些尖晶石结构的 Li M2O4(M=Ti,V,Mn)化合物中,氧原子按照 ABCABC进行立方密堆积。Li Mn2O4为例的尖晶石结构如图 1.4 所示,锂离子占据氧原子的 8a 四面体,过渡金属离子会占据氧原子的 16d 八面体位置,其具体的排列情况由静电引力、库伦斥力和离子半径等因素决定。
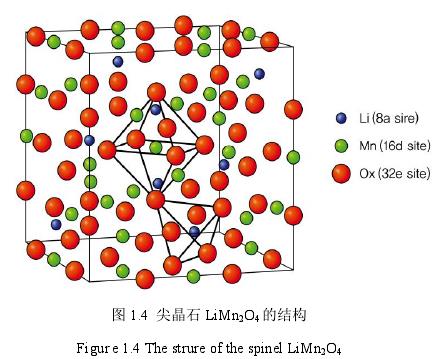
当 3+或 4+的 3d 过渡金属离子半径和氧原子半径的比值在 0.476 到 0.702 或者 0.492 到 0.591 之间时,过渡金属离子位于八面体位置。实际上在尖晶石和层状结构中,所有的过渡金属离子都占据着八面体位置。尖晶石结构 Li M2O4如同层状 Li MO2
化合物中 M-M 的相互排斥作用一样,共边的八面体结构排列具有类似的库伦排斥力,使得尖晶石结构的材料也拥有良好的离子电导率。
C.
橄榄石型化合物在一般的 M2XO4橄榄石结构中,在六方密堆积的氧原子形成的空位中一半的八面体位置上是 M,而 X 占据八分之一的四面体位置,这与立方尖晶石结构类似。若 X 的离子半径较小,橄榄石结构会优于尖晶石结构形成。表
1.1
对橄榄石结构和尖晶石结构进行了对比。在橄榄石型化合物中,两种不同的八面体形成了均匀的结构,从而允许锂离子在一维方向上进行扩散。在橄榄石型化合物中,由于氧原子的强烈键和作用,其结构具有较高的热稳定性。但是在锂离子脱出和嵌入过程中会造成橄榄石型化合物的结构发生变化,所以以其为正极材料的锂离子电池的容量和倍率性能都相对较差。
目前最常用的橄榄石型正极材料 Li Fe PO4与 Li Co O2相比较而言,Fe 的含量比 Co 的含量更丰富,并且具有更环保和价格便宜等优势。Li Fe PO4是由 Li Fe PO2衍生来的,但是由于 Li Fe PO2的工作电压只有 3.2V,导致其无法满足实际应用。然而通过聚阴离子 XO4y-(X=S,P,As;y=2,3)取代,其电压也可以提高到 3.4V。
Li Fe PO4的理论密度是 3.6g/cm³,理论比容量是 170m Ah/g,平均工作电压是 3.4V,不足以分解电解液,与此同时能够提供一定的能量密度,因此 Li Fe PO4能够作为一种优秀的正极材料运用于动力汽车中。但其最大的缺点就在于电导率低,这是
橄榄型化合物的共性,电导率低会导致长期的充放电过程产生明显的极化作用,从而使其容量显著下降,研究人员发展了各种方法来提高 Li Fe PO4的倍率性能。



